اخیرا کشفهای بسیاری در زمینهی شیمی صورت گرفته است که با دانش معمول ما متفاوت است. به تازگی دانشمندان توانستهاند ترکیبی جدید از هلیوم بسازند.
اگر شیمی دبیرستان را به یاد داشته باشید، میدانید که هلیوم گازی نجیب است، کمترین میزان واکنشپذیری را در جدول تناوبی دارد و چون بیرونیترین لایهی الکترونی آن پر است، با دیگر عنصرها واکنش نمیدهد تا ترکیبهای پایدار ایجاد کند.
دیگر گازهای نجیب تحت فشار زیاد ترکیباتی را ایجاد کردهاند؛ اما تاکنون هلیوم ترکیب پایداری ایجاد نکرده بود. دانشمندان گزارش دادهاند که ترکیبی ساختهاند که به نظر میرسد ترکیب پایداری از هلیوم و سدیم باشد. ساخت این ترکیب بسیاری از فرضیات اساسی شیمی مدرن را زیر سوال میبرد.
آدام پاپاو از دانشگاه یوتا و از اعضای تیم میگوید:
وقتی فشارهای بالا را اعمال میکنید، شیمی تغییر میکند. این فشارهای بالا در داخل زمین و در سیارههای متفاوتی مانند زحل قابل دستیابی است. اما این پژوهش بسیاری از معادلات را به هم میزند.
هلیوم دومین عنصر فراوان در جهان است و در بالای گروه شش عضوی گازهای نجیب قرار گرفته است. آخرین لایهی الکترونی این عنصرها که عامل واکنشپذیری آنها هم است، پر است؛ بنابراین این گازها با دیگر عنصرها واکنش نمیدهند و ترکیبی ایجاد نمیکنند.
این گازها از این جهت نجیب نامیده میشوند که با عنصرهای دیگر واکنش نمیدهند. البته در شرایط ویژه میتوانید نشانههایی از واکنشپذیری آنها را مشاهده کنید. گازهای نجیب به دو دسته تقسیم میشوند: گروه اول شامل کریپتون، زنون و رادون تا حدودی واکنشپذیر شناخته میشوند؛ گروه دیگر شامل آرگون، نئون و هلیوم کاملا واکنشناپذیر محسوب میشوند.
پژوهشگران راههایی برای اتصال هلیوم به دیگر عنصرها یافته بودند؛ اما تاکنون نتایج ناپایدار بودند. از برهمکنشهای هلیوم با دیگر عنصرها میتوان به پیوند واندروالس اشاره کرد. نیروی واندروالس، جزو نیروهای جاذبه یا دافعه است که بدون نیاز به پیوند کووالانسی یا یونی شکل میگیرد. در واقع پیوند کووالانسی یا یونی، با اشتراکگذاری الکترونها بین اتمها شکل میگیرد تا یک مولکول ایجاد شود. اما پیوند واندروالسی، نیروی ضعیفتری است که بین مولکولها یا اتمهای منفرد شکل میگیرد، بی آنکه مولکولی ایجاد کند.
پیوند واندروالس بین هلیوم و دیگر اتمها وجود دارد. در دماهای بسیار پایین، هلیوم میتواند “مولکولهای واندروالسی” ایجاد کند. مولکولهای واندروالسی خوشههایی از اتمها یا مولکولها هستند که نیروی اتصال دهندهی آنها بسیار ضعیف بوده و ناپایدار نیز هستند.
هلیوم واکنش پذیر نیست؛ زیرا آرایش الکترونی لایهی بیرونی آن کامل است. در واقع آرایش الکترونی لایهی آخر آن جایی برای به اشتراکگذاری الکترون با دیگر اتمها ندارد تا پیوند ایجاد شود. اما این شرایط روی سطح زمین برقرار هستند.
هلیوم یکی از فراوانترین عنصرهای هستی است و در شکلگیری ستارهها و سیارههای غولپیکر نقش دارد. هلیوم در فضا و در هستهی زمین، بسیار متفاوت عمل میکند. اکنون پژوهشگران موفق شدهاند تا نخستین شواهد از این رفتار عجیب را بیابند.
آلکس بولدروف، یکی از اعضای تیم از ایالت یوتا میگوید:
فشارهای خیلی بالا، مثل فشار مرکز کرهی زمین یا فشار سیارههای گازی همسایه کاملا شیمی هلیوم را تغییر میدهد.
پژوهشگران از یک مدل کامپیوتری پیشبینیکنندهی ساختار کریستال استفاده کردند تا پیشبینی کنند که آیا در فشارهای خیلی بالا، ترکیب پایدار هلیوم-سدیم میتواند شکل بگیرد یا خیر. آنها سپس این ترکیب، یعنی Na2He را در یک سندان الماس ساختند.
این سندان الماس امکان دستیابی به فشار ۱.۱ میلیون برابر فشار اتمسفری زمین را ممکن میسازد. بولدروف میگوید که این نتایج غیر قابل انتظار بودند و آنها بیش از دو سال تلاش کردند تا بازخوانها و سردبیران ساینس را متقاعد کنند که نتایج آنها را چاپ کنند.
تیم با توجه به این نتایج پیشبینی میکند که تحت شرایط فشار ۱۰ میلیون برابر فشاری که آنها به آن دست یافته اند، سدیم به راحتی با گاز هلیوم ترکیب میشود و ترکیب Na2He را ایجاد میکند. عجیب است که این ترکیب بدون هیچ پیوند شیمیایی که آنها را در کنار هم نگاه دارد، ایجاد میشود.
ژائو دانگ از دانشگاه نانکای در چین در بیانیهای گفته است:
ترکیبی که یافتهایم، بسیار ویژه است: اتمهای هلیوم پیوند شیمیایی تشکیل ندادهاند؛ اما حضور آنها برهمکنشهای شیمایی بین اتمهای سدیم را تغییر داده و الکترونها را داخل حفرههای ساختار مکعبی مستقر کرده است.
در تصویر زیر، ساختار کریستالی Na2He را میبینید. اتمهای سدیم به رنگ بنفش و اتمهای هلیوم سبز هستند. الکترونها فضاهای قرمز بین آنها هستند.

ساخت ترکیب پایداری از هلیوم توسط دانشمندان شیمی
پاپوف میگوید که پیوند تشکیل شده، پیوندی واقعی مانند پیوندهای یونی یا کووالانسی نیست؛ اما این هلیوم است که ساختار را پایدار کرده است. اگر اتمهای هلیوم را حذف کنید، این ساختار پایدار نخواهد بود. در اینجا چند بازنمود دیگر از این ترکیب را میبینید. در تصویر سمت چپ، سدیم صورتی و هلیوم سفید است. در تصویر سمت راست، مکعبهای سدیم و هلیوم خاکستری و الکترونها قرمز هستند:
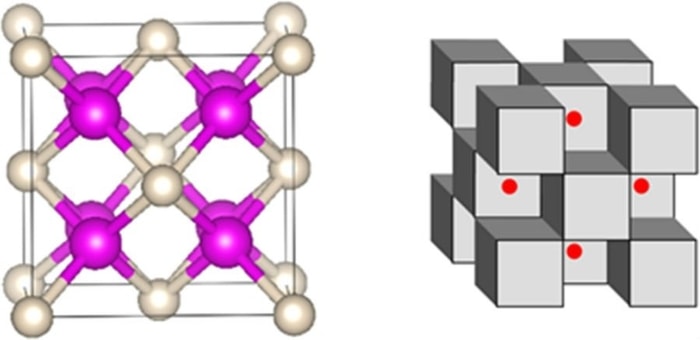
ساخت ترکیب پایداری از هلیوم توسط دانشمندان شیمی



 خرید واکس داشبورد
خرید واکس داشبورد شیونده خودرو نانو پودر تاچ لس محصولی بی نظیر و پرکاربرد
شیونده خودرو نانو پودر تاچ لس محصولی بی نظیر و پرکاربرد خرید بهترین محصولات کارواش و شوینده خودرو
خرید بهترین محصولات کارواش و شوینده خودرو شوینده خودرو نانوپودر تاچ لس شیمی صنعت تبریز
شوینده خودرو نانوپودر تاچ لس شیمی صنعت تبریز خرید شوینده خودرو ارزان
خرید شوینده خودرو ارزان هستهی زمین تنها ۱ میلیارد سال قدمت دارد
هستهی زمین تنها ۱ میلیارد سال قدمت دارد دانشمندان نظریهی جدیدی برای منشأ شکلگیری آب در زمین ارائه کردند
دانشمندان نظریهی جدیدی برای منشأ شکلگیری آب در زمین ارائه کردند تولید محصولات گوگل با مواد بازیافتی
تولید محصولات گوگل با مواد بازیافتی ثبت بزرگترین رکورد صاعقه در جهان به طول ۷۰۰ کیلومتر در برزیل
ثبت بزرگترین رکورد صاعقه در جهان به طول ۷۰۰ کیلومتر در برزیل تجزیه آب بوسیله نوعی الکترود و با کمک نانوذرات امکان پذیر شد
تجزیه آب بوسیله نوعی الکترود و با کمک نانوذرات امکان پذیر شد خرید محصول گرافن کوانتوم دات
خرید محصول گرافن کوانتوم دات همه چیز درباره کوانتوم دات گرافن
همه چیز درباره کوانتوم دات گرافن معرفی و کاربرد محصول گرافن کوانتوم دات
معرفی و کاربرد محصول گرافن کوانتوم دات آب صابون نانو چیست؟
آب صابون نانو چیست؟ تولید نوعی پارچه با قابلیت خنثی سازی اثر تسلیحات شیمیایی
تولید نوعی پارچه با قابلیت خنثی سازی اثر تسلیحات شیمیایی آب صابون , آب صابون نانو
آب صابون , آب صابون نانو روش های مختلف ماشین کاری و تاثیر آب صابون
روش های مختلف ماشین کاری و تاثیر آب صابون سیاه ترین رنگ تجاری با استفاده از نانو لوله های کربنی تولید شد
سیاه ترین رنگ تجاری با استفاده از نانو لوله های کربنی تولید شد بررسی مزایا و معایب رویکرد استارت آپ ناب
بررسی مزایا و معایب رویکرد استارت آپ ناب کارآفریی چیست و راهکارهای موفقیت در کارآفرینی
کارآفریی چیست و راهکارهای موفقیت در کارآفرینی کشف اولین جاندار چند سلولی که بدون اکسیژن زندگی میکند
کشف اولین جاندار چند سلولی که بدون اکسیژن زندگی میکند بیوگرافی پدر شیمی مدرن ، رابرت بویل
بیوگرافی پدر شیمی مدرن ، رابرت بویل چرا باید محصولات دکترواش را خریداری کنیم؟
چرا باید محصولات دکترواش را خریداری کنیم؟ کشف آنتی بیوتیک های قدرتمند توسط هوش مصنوعی
کشف آنتی بیوتیک های قدرتمند توسط هوش مصنوعی تهیه آب آشامیدنی از هوای خشک
تهیه آب آشامیدنی از هوای خشک